 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“设氨水的解离平衡常数为。浓度为mol·L-1的氨水溶液,若将其用水稀释一倍,则溶液中OH-的浓度(mol·L-1)为()ABCD24、已知(Ag3PO4)=1”相关的问题
更多“设氨水的解离平衡常数为。浓度为mol·L-1的氨水溶液,若将其用水稀释一倍,则溶液中OH-的浓度(mol·L-1)为()ABCD24、已知(Ag3PO4)=1”相关的问题
第1题
1.![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/8bc30b4-chaoxing2016-284157.jpeg) 时,
时,![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/9e34d4c-chaoxing2016-284158.jpeg) 的溶度积为
的溶度积为![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/69637ba-chaoxing2016-284159.jpeg) ,氨水的解离常数为
,氨水的解离常数为![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/0ee2b26-chaoxing2016-192990.jpeg) ,向200mL浓度为0.2 mol/L的
,向200mL浓度为0.2 mol/L的![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/6f4afec-chaoxing2016-284160.jpeg) 溶液中加入200mL浓度为0.2 mol/L的氨水和5.0克
溶液中加入200mL浓度为0.2 mol/L的氨水和5.0克![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/50c5ca3-chaoxing2016-192760.jpeg) 固体,通过计算说明有无
固体,通过计算说明有无![1. [图]时,[图]的溶度积为[图],氨水的解离常数为[图],...1. 时,的溶度积为,氨水的解](http://static.jiandati.com/9e34d4c-chaoxing2016-284158.jpeg) 沉淀生成?
沉淀生成?
第2题
电导他用0.01mol·dm-3标准KCl溶液标定时,其电阻为189Ω,用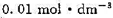 的氨水溶液测其电阻值为2460Ω。用下列该浓度下的摩尔电导率数据计算氨水的标准解离平衡常数。
的氨水溶液测其电阻值为2460Ω。用下列该浓度下的摩尔电导率数据计算氨水的标准解离平衡常数。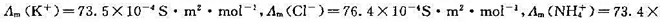 ,
,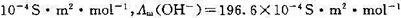 设活度因子均为1。
设活度因子均为1。
第3题
在298K时,醋酸HAc的解离平衡常数Ka=1.8×10-5,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。
1
)设溶液是理想的,活度系数均为
1
(
2
)
用德拜
-
休格尔极限公式计算出
γ
的值再计算电离度。
设未离解的
HAc
的活度系数为
1
。
已知
:A
=
0.509 (mol
·
kg
1
)
1/2

第4题
A.Km/Vmax为200
B.该酶的转换数是100min-1
C.酶底物复合物解离成酶和产物的平衡常数 0.005mol/L
D.当底物浓度为0.005mol/L时,反应速度为5mol/min
E.反应速度随底物浓度增加呈线性增加
第5题
A.Km/Vmax为200
B.该酶的转换数是100min-1
C.酶底物复合物解离成酶和产物的平衡常数 0.005mol/L
D.当底物浓度为0.005mol/L时,反应速度为5mol/min
E.反应速度随底物浓度增加呈线性增加
第6题
A.各点溶液中的阳离子浓度总和大小关系:d>c > b > a
B.常温下,R- 的水解平衡常数数量级为10 -9
C.点和d点溶液中,水的电离程度相等
D.点的溶液中,微粒浓度关系
第7题
电导池用0.01mol·dm-3标准KCl溶液标定时,其电阻为189Ω,用0.01mol·dm-3的氨水溶液测其电阻值为2460Ω。用下列该浓度下的摩尔电导率数据计算氨水的标准解离平衡常数。Am(K+)=73.5×10-4S·m2·mol-1,Am(Cl-)=76.4×10-4S·m2·mol-1,Am(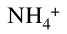 )=73.4×10-4S·m2·mol-1,Am(OH-)=196.6×10-4S·m2·mol-1,设活度因子均为1。
)=73.4×10-4S·m2·mol-1,Am(OH-)=196.6×10-4S·m2·mol-1,设活度因子均为1。
第9题
0.2 mol/L的氨水和0.2 mol/L等体积的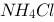 水溶液混合,溶液中的
水溶液混合,溶液中的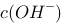 = ? mol/L。已知氨水的解离常数为
= ? mol/L。已知氨水的解离常数为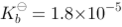
A、0.1
B、0.2
C、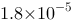
D、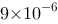
第10题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
